
W lutym 1994 roku oddział ratunkowy jednego z kalifornijskich szpitali (zdjęcie wiodące) przyjął 31-letnią Glorię Ramirez, cierpiącą na raka szyjki macicy. Choć poważnie chora pacjentka wkrótce zmarła, nie byłoby w tym nic niezwykłego – gdyby nie to, co działo się w trakcie udzielania jej pomocy i później. Trójka pracowników szpitala zajmujących się Glorią Ramirez straciła przytomność, inni doznali trudności w oddychaniu i drgawek mięśniowych. Jedna osoba spędziła nawet dwa tygodnie na oddziale intensywnej opieki medycznej (OIOM, ang. ICU – Intensive Care Unit).
Późniejsze dochodzenie wskazało, że przyczyną tego wypadku był dimetylosulfotlenek (DMSO) przyjmowany przez chorą jako środek przeciwbólowy. Trzeba też zauważyć, że „medycyna” alternatywna proponuje ten związek jako lek na raka, co oczywiście nie ma żadnego potwierdzenia w badaniach klinicznych. Powoduje natomiast zagrożenie dla chorych przyjmujących niektóre rodzaje chemioterapii, gdyż DMSO zakłóca działanie leków przeciwrakowych będących pochodnymi platyny.
Podczas przewozu Ramirez do szpitala ratownicy medyczni podali jej tlen, który utlenił DMSO do silnie trującego siarczanu(VI) dimetylu. Ten lotny związek znalazł się w powietrzu otaczającym pacjentkę, a także wydzielał z pobranych od niej próbek krwi.

Dimetylosulfotlenek (CH₃)₂SO jest organicznym związkiem siarki z grupy sulfotlenków, mającym dość szerokie zastosowanie. Jest to bezbarwna i bezwonna ciecz o tw. 189°C, będąca dobrym rozpuszczalnikiem polarnym aprotycznym. „Aprotyczny” oznacza, że w jego cząsteczce brak atomów wodoru, które mogłyby oddysocjować jako protony. Obecność grup metylowych powoduje, że w DMSO dobrze rozpuszczają się związki niepolarne. Jednak sam DMSO ma polarną cząsteczkę, a obecność atomu tlenu z niewiążącymi parami elektronowymi oznacza możliwość przyłączania protonu i tworzenia wiązań donorowo-akceptorowych (jako donor pary elektronowej). Dzięki temu w DMSO dobrze rozpuszczają się również związki polarne.
Czysty dimetylosulfotlenek jest nietoksyczny. Związek ten jest znany od XIX wieku i został otrzymany po raz pierwszy przez rosyjskiego chemika Aleksandra Zajcewa w 1866 roku.
Mimo obecności trzech podstawników przy atomie siarki cząsteczka DMSO nie jest płaska. Wynika to z faktu, że siarka jest w tym związku czterowartościowa, co oznacza, że na utworzenie wiązań (kowalencyjnych) zużyła tylko cztery z sześciu swoich elektronów walencyjnych. Dwa ostatnie tworzą parę niewiążącą, przez co liczba hybrydyzacji atomu siarki jest równa 4 (3+1 – suma liczby podstawników i liczby par niewiążących). To zaś oznacza, że atom siarki jest w stanie hybrydyzacji sp³, a cząsteczka DMSO ma kształt piramidy trygonalnej (trójkątnej).
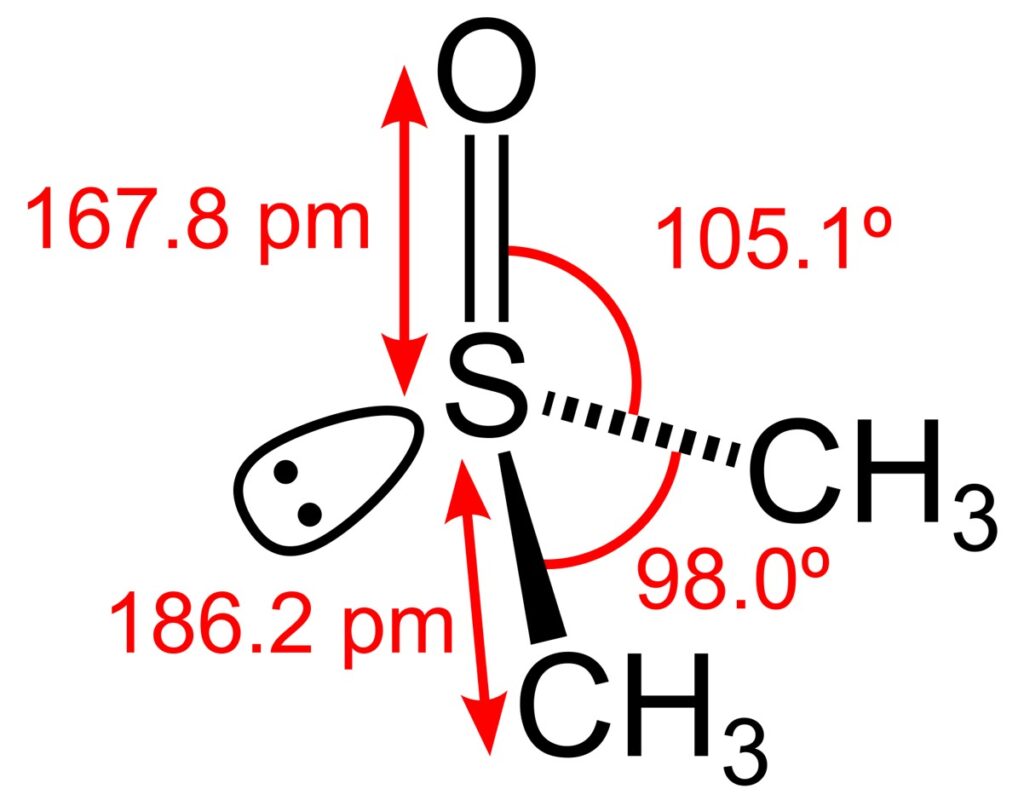
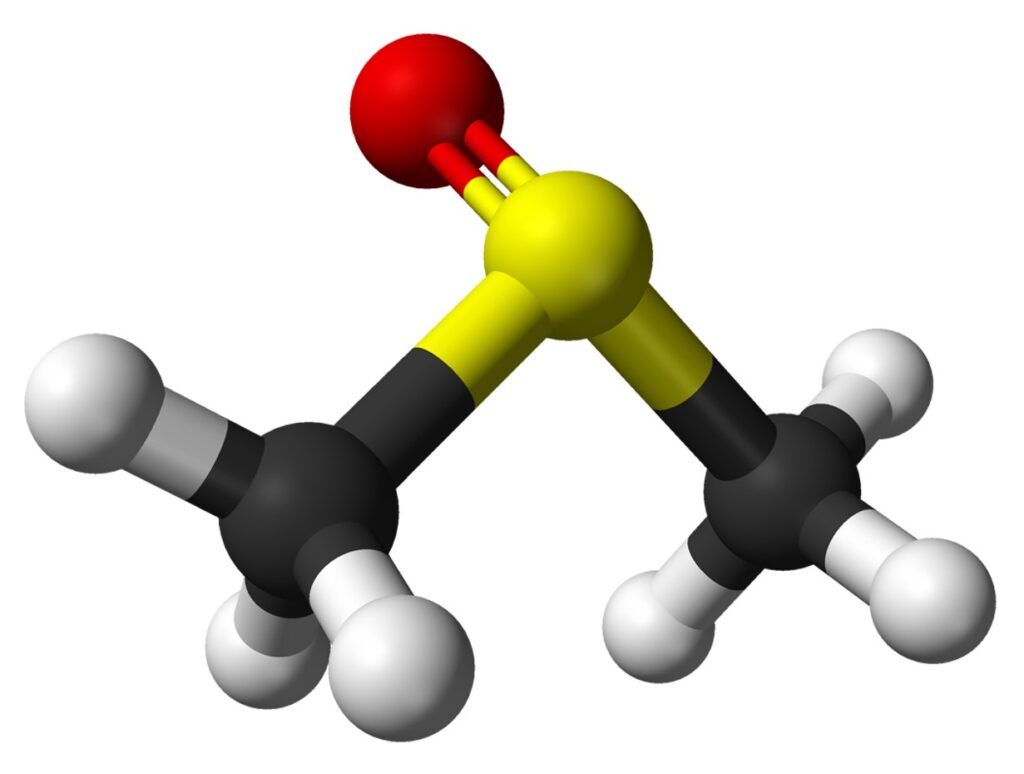
Dimetylosulfotlenek jest stosowany przede wszystkim jako rozpuszczalnik w laboratorium chemicznym oraz podczas badania leków in vitro i in vivo. Deuterowana forma DMSO, w której sześć atomów wodoru zastąpiono atomami deuteru, jest używana jako rozpuszczalnik w badaniach NMR (magnetycznego rezonansu jądrowego). W medycynie DMSO służy jako nośnik niektórych leków, ponieważ łatwo przenika przez skórę; ma też zastosowanie jako podawany zewnętrznie środek przeciwbólowy. Co ciekawe, kontakt z DMSO powoduje wrażenie odczuwania smaku czosnku.
Z kolei siarczan(VI) dimetylu (CH₃)₂SO₄ albo (CH₃O)₂SO₂, należący do estrów nieorganicznych, jest silną trucizną o LC₅₀ rzędu kilkudziesięciu ppm (części na milion; dostępne dane dotyczą szczurów, myszy, świnek morskich i człowieka). Ma on postać oleistej, bezbarwnej cieczy o zapachu cebuli (tt. –32°C, tw. 188°C). Jest bardzo reaktywny (np. reaguje z wodą w warunkach normalnych), dzięki czemu może służyć jako bardzo skuteczny odczynnik metylujący fenole, aminy i tiole. Przemysł chemiczny preferuje siarczan(VI) dimetylu w tej roli, gdyż można go łatwo otrzymać w reakcji tritlenku siarki z eterem dimetylowym.
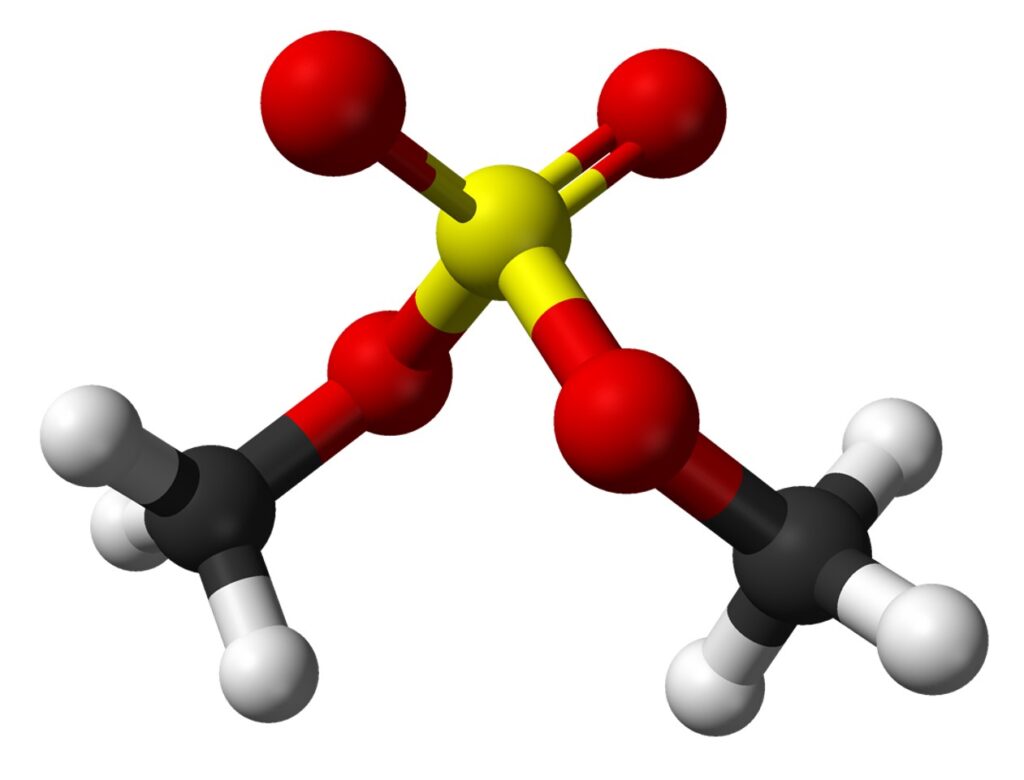
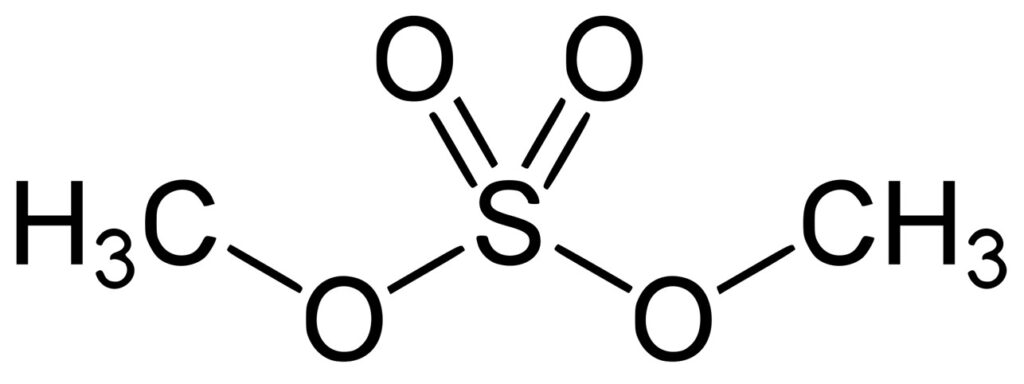
Związek ten jest znany od początku XIX wieku, dokładniej opisali go francuscy chemicy Dumas i Péligot w 1835 roku. W okresie I wojny światowej Niemcy i Francja badały możliwość użycia siarczanu(VI) dimetylu jako środka bojowego. Substancja ta jest nie tylko bardzo toksyczna, ale także żrąca i niebezpieczna dla środowiska; ma też działanie rakotwórcze i mutagenne. W organizmie Glorii Ramirez powstał prawdopodobnie z dimetylosulfonu (CH₃)₂SO₂, do którego utlenił się DMSO.
Post pierwotnie opublikowany na facebookowej grupie „Chemia dla nauczycieli” wydawnictwa Nowa Era.
[źródła: https://en.wikipedia.org/wiki/Death_of_Gloria_Ramirez; https://en.wikipedia.org/wiki/Dimethyl_sulfoxide; https://en.wikipedia.org/wiki/Dimethyl_sulfate]
[źródła ilustracji: Google Maps; User:Benjah-bmm27 – File:DMSO-2D-dimensions.png, Public Domain, https://commons.wikimedia.org/w/index.php?curid=26559919; Ben Mills – Own work, Public Domain, https://commons.wikimedia.org/w/index.php?curid=4418009; Σ64 – Own work, CC BY 3.0, https://commons.wikimedia.org/w/index.php?curid=26276169; User:Calvero – Selfmade with ChemDraw., Public Domain, https://commons.wikimedia.org/w/index.php?curid=998585]