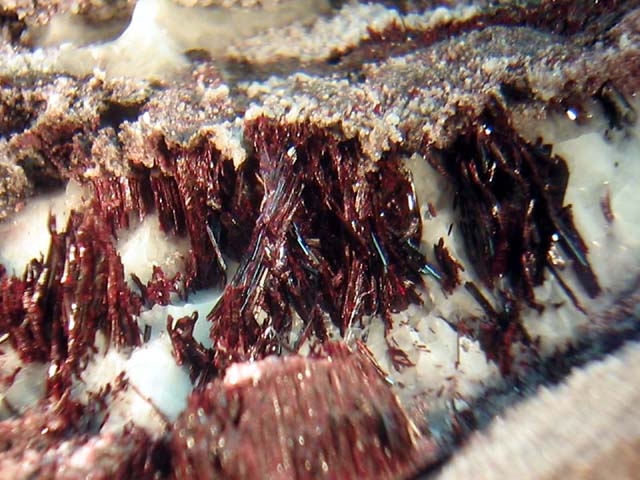
Piemontyt {Ca₂}{Al₂Mn³⁺}(Si₂O₇)(SiO₄)O(OH) jest minerałem z grupy epidotu (chemicznie – sorokrzemianem pod względem składu podobnym do klinozoisytu), o czerwonym lub ciemnoczerwonym zabarwieniu, za które odpowiada jon manganu(III). Czy to nie dziwne, że wystarczy różnica jednego elektronu, by związki tego samego metalu aż tak bardzo różniły się barwą? Związki manganu(II) są bowiem bezbarwne w roztworze wodnym, a w stanie stałym co najwyżej jasnoróżowe.
Tu zaczyna się wycieczka do krainy kwantów – kto źle się czuje w ich towarzystwie, może przeskoczyć cały fragment 🙂
Aby odpowiedzieć na to pytanie, trzeba poznać pewne podstawowe wiadomości z dziedziny spektroskopii. W przypadku takich substancji za barwę odpowiadają elektrony walencyjne. Mangan, jako pierwiastek siódmej grupy, ma ich siedem, zatem jon Mn²⁺ ma pięć elektronów walencyjnych (bo dwa utracił, stąd ładunek +2), a jon Mn³⁺ – cztery (7–3). Elektrony te znajdują się na podpowłoce walencyjnej d, która, jeśli mówimy o jonach w roztworze wodnym, jest podzielona (rozszczepiona) na dwa podpoziomy: niższy obejmuje trzy orbitale, wyższy dwa. W przypadku jonu manganu(II) elektrony są rozłożone następująco:
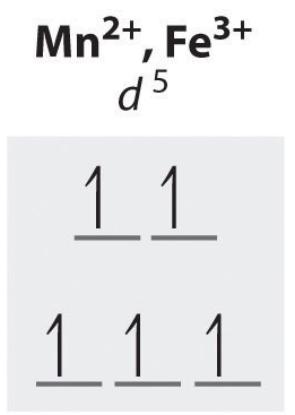
Czyli w takim jonie znajduje się pięć elektronów niesparowanych. Za barwę odpowiadają przejścia elektronów z niższego podpoziomu na wyższy. Jednak w przypadku takiej konfiguracji (nazywa się ona wysokospinową, ponieważ ma maksymalną możliwą liczbę elektronów niesparowanych) przejście elektronu z dolnego poziomu na górny wiązałoby się ze zmianą liczby elektronów niesparowanych: elektron wzięty z dolnego poziomu musiałby się sparować z jednym z elektronów z górnego poziomu, przez co liczba elektronów niesparowanych zmalałaby z 5 do 3. Takie zjawisko jest z różnych względów niezmiernie utrudnione (w spektroskopii mówi się, że jest to przejście zabronione, co nie ma jednak charakteru absolutnego, podobnie jak zakaz przechodzenia na czerwonym świetle). Wobec tego barwa wynikająca z tego przejścia ma znikome natężenie – do tego stopnia, że związek w niezbyt stężonym roztworze może wydawać się bezbarwny.
Inaczej jest w przypadku jonu manganu(III), który ma elektrony walencyjne rozłożone następująco:
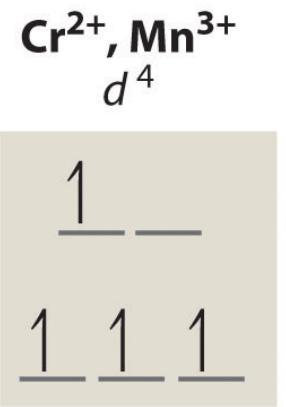
Tu co prawda liczba niesparowanych elektronów jest również maksymalna (jak na tę liczbę elektronów walencyjnych). Jednak elektron, który przeskoczyłby z dolnego poziomu na górny, znalazłby sobie tam wolne miejsce i nie musiałby się parować z elektronem, który już tam siedzi. Zatem liczba elektronów niesparowanych nie zmieniłaby się – byłoby ich nadal cztery, jak na tym rysunku. Takie przejście elektronowe nie jest już tak mocno zabronione, więc powstające dzięki niemu zabarwienie może być bardziej intensywne. I dlatego minerał zawierający jon Mn³⁺ może być soczyście czerwony.
Koniec wycieczki do krainy kwantów, wracamy do piemontytu.
Jak łatwo się domyślić, nazwa tego minerału pochodzi od Piemontu, krainy we Włoszech. Żeby nie było jednak tak całkiem prosto, znany od połowy XVIII wieku piemontyt zwany był kolejno czerwoną magnezją (od góry zwanej Magnezją pochodzi nazwa zarówno magnezu, jak i manganu), krzemonośnym fioletowym tlenkiem manganu, manganonośnym epidotem i piemonckim braunsztynem (dziś braunsztynem nazywa się minerał zawierający inny związek manganu, MnO₂). Tę ostatnią nazwę skrócono w końcu do piemontytu.
Piemontyt jest dość twardy (6-6,5), a jego gęstość wynosi ok. 3,5 g/cm³. Powstaje wskutek metamorfizmu złóż manganu. Nie jest zbyt rozpowszechniony, ale znaleziono go na wszystkich kontynentach (niestety ominął Europę Środkową). Odkryty został w kopalni Prabornaz we Włoszech.
Minerał ten występuje głównie w postaci drobnokrystalicznej. Z uwagi na jego często fioletowoczerwone zabarwienie, niektóre egzemplarze wyglądają jak mięsko (ostatnie zdjęcie).
Piemontyt bywa wykorzystywany do wyrobu biżuterii, wobec czego zajmują się nim również strony kamiennomagiczne. Jest to mianowicie kamień czakry serca i pomaga słyszeć, co inne serca mają do powiedzenia. Łączy się duchowo z radością i duchowym samoleczeniem, zwalcza smuteczki.
[zdjęcia za pośrednictwem strony mindat.org, autorzy: OT.Ljostad, Giovanni Fraccaro, Jerry A. Bird, Michael C. Roarke, Ben Kirchner, Enrico Bonacina, Michael D. Cline, Cristian Biagioni; ostatnie zdjęcie Dakota Matrix]