
W ciągu kilku ostatnich tygodni kilkakrotnie na różnych stronach internetowych pojawiły się artykuły na temat możliwości znalezienia w kosmosie nieznanych nam pierwiastków. Zwłaszcza autorzy nagłówków, którzy zwykle niewiele rozumieją poza koniecznością generowania clickbaitów, pozwalali sobie na daleko idące sensacje. Opierały się one na rzeczywiście niezwykłym doniesieniu – o odkryciu planetoid, których gęstość przekracza gęstość osmu, pierwiastka rekordowego pod tym względem (22,6 g/cm³; prócz osmu potwierdzoną gęstość większą od 20 mają jeszcze neptun, ren, platyna i iryd). Stąd już niedaleko było do wniosku, że owe planetoidy (zwane też asteroidami) muszą zawierać nowe pierwiastki, nieznane dotąd ludzkości. Spróbuję ustalić, ile w tym prawdy i sensu.

Obecnie uważa się, iż liczba odkrytych lub wytworzonych przez człowieka pierwiastków wynosi 118. Tak przy okazji, oznacza to, że układ okresowy zawiera siedem „kompletnych” okresów i kolejne pierwiastki powinny zapoczątkować nowy okres, ósmy. Nie jest to tylko formalność polegająca na dorysowaniu kolejnego wiersza tabelki – pierwiastki ósmego okresu będą obsadzać elektronami ósmą powłokę o symbolu R (we wcześniejszych okresach obsadzane są kolejno powłoki K, L, M, N, O, P, Q), a to może – powtarzam, może – pociągnąć za sobą jakieś nietypowe właściwości.
Niestety wzrost ciężaru jądra atomowego powoduje spadek jego trwałości (a przy okazji – nie ma bezpośredniego przełożenia na gęstość pierwiastka, która jest parametrem makroskopowym i zależy też od budowy kryształu pierwiastka). Aktualnie pierwiastkiem, który ma „najcięższe” jądro występujące w przyrodzie, jest uran. Jądro atomu uranu zawiera 92 protony i jest otoczone przez 92 elektrony, ale prócz tego może też zawierać neutrony. Tyle tylko, że liczba neutronów, jakie mogą znajdować się w jądrze, nie jest ściśle określona i – zwłaszcza u ciężkich pierwiastków – może mieścić się w sporym przedziale.
Jądra atomowe mające jednakową liczbę protonów (czyli będące jądrami tego samego pierwiastka), ale różniące się liczbą neutronów nazywają się izotopami. Suma protonów i neutronów nazywa się liczbą masową; właśnie wartość tej liczby identyfikuje poszczególne izotopy (tak jak liczba protonów, zwana liczbą atomową, identyfikuje pierwiastki). Na przykład węgiel (liczba atomowa 6) może występować w przyrodzie w postaci izotopów o liczbie masowej 12, 13 i 14.
| Symbol | Liczba protonów = liczba atomowa | Liczba neutronów | Liczba masowa | Rozpowszechnienie | Okres półtrwania |
| ¹²C | 6 | 6 | 12 | 98,9% | trwały |
| ¹³C | 6 | 7 | 13 | 1,06% | trwały |
| ¹⁴C | 6 | 8 | 14 | 0,0000000001% | 5700 lat |
C-12, inaczej oznaczany jako ¹²C, to „zwykły” węgiel i (jak wskazuje powyższa tabela) jest go w przyrodzie najwięcej. C-14, inaczej ¹⁴C, jest nietrwałym izotopem, którego atomy mogą ulegać samorzutnemu rozpadowi (zmieniając się w atomy azotu). Proces ten zachodzi w określonym tempie, dzięki czemu wykorzystujemy pomiary zawartości poszczególnych izotopów różnych pierwiastków do datowania – przedmiotów wykonanych przez człowieka, szczątków, wykopalisk, a nawet skał i minerałów. W przypadku datowania na podstawie ilości izotopu C-14 mówimy o metodzie radiowęglowej, najsłynniejszej, opracowanej jako pierwsza, ale nadającej się do badania próbek mających nie więcej niż 50 tysięcy lat.
Izotop ¹³C też się przydaje. Jako odmiana o nieparzystej liczbie masowej może być wykorzystywany w jednej z odmian magnetycznego rezonansu jądrowego, czyli NMR. Jest to całkowicie bezpieczna, nieinwazyjna technika, która umożliwia badanie wnętrza obiektów – swoiste „prześwietlanie”, choć działa na zupełnie innej zasadzie niż rentgen. Rezonans jądrowy jest wykorzystywany w medycynie, aczkolwiek tam nazywa się go MRI (ang. Magnetic Resonance Imaging, obrazowanie rezonansem magnetycznym), żeby nie straszyć wrażliwych pacjentów jądrami. Istnieje kilka rodzajów NMR: wodorowy (protonowy), węglowy, fluorowy, fosforowy i inne. Ale nad tym nie będę się tu rozwodzić, choć to bardzo ciekawy temat.
Nietrwałe izotopy pierwiastków mogą wytrzymywać dłużej lub krócej – opisuje to parametr zwany okresem lub czasem półtrwania albo półżycia, po angielsku half-life (czyli termin dobrze znany miłośnikom gier komputerowych). W ostatniej kolumnie tabeli z izotopami węgla można znaleźć informację, że okres półtrwania C-14 wynosi 5700 lat. Oznacza to, że z dowolnej porcji atomów węgla-14 po 5700 latach zostanie połowa, po następnych 5700 latach – połowa połowy, czyli jedna czwarta, i tak dalej. Nie jest istotne, ile atomów było na początku, nie jesteśmy też w stanie przewidzieć, które konkretnie atomy przetrwają ani kiedy rozpadnie się dany atom. Procesy przemian radioaktywnych zachodzą zgodnie z zasadami mechaniki kwantowej, a zatem mają charakter statystyczny (fizycy mówią „stochastyczny”, czyli losowy).
Wspomniany wcześniej uran ma 28 izotopów o wszystkich liczbach masowych od 214 do 242, jednak żaden z nich nie jest trwały. Począwszy od pierwiastka nr 83, czyli bizmutu, nie znamy żadnych trwałych izotopów. Siły elektrostatycznego odpychania między protonami o ładunku dodatnim stają się tak wielkie, że nie pomaga rozcieńczanie protonów pozbawionymi ładunku neutronami i silne oddziaływania jądrowe w końcu nie dają rady utrzymać jądra w kupie. Co prawda w przypadku bizmutu wytrzymują dość długo, bo główny izotop tego pierwiastka ma okres półtrwana 20 000 000 000 000 000 000 lat (20 milionów bilionów, co dość wyraźnie przekracza wiek Wszechświata, szacowany obecnie na niecałe 14 miliardów lat).
Dwa najtrwalsze izotopy uranu też są dość wytrzymałe: najpowszechniejszy, U-238, ma okres półtrwania ok. 4,5 miliarda lat, a ten najważniejszy, U-235 (surowiec do produkcji paliwa jądrowego oraz, niestety, bomb atomowych) – ok. 700 milionów. Oznacza to, że gdy już powstaną, to są w stanie przetrwać naprawdę długo.
Ale dlaczego ja się nad tym rozwodzę, skoro miałem pisać o perspektywach znalezienia w kosmosie nowych pierwiastków? Ano dlatego, że im dłużej wytrzymują atomy danego pierwiastka, tym łatwiej go odkryć lub otrzymać. A z okresem półtrwania u najnowszych pierwiastków nie jest najlepiej. Jeśli przyjrzeć się temu parametrowi u 15 najcięższych znanych pierwiastków, widać, że poruszamy się w przedziałach co najwyżej godzinowych (dokładne dane w tabeli poniżej, podaję wartości tylko dla potwierdzonych izotopów w stanie podstawowym).
| Nazwa pierwiastka | Liczba atomowa | Symbol najtrwalszego izotopu | Okres półtrwania |
| Rutherford | 104 | ²⁶⁷Rf | 1,3 h |
| Dubn | 105 | ²⁶⁸Db | 16,0 h |
| Seaborg | 106 | ²⁷¹Sg | 1,9 min |
| Bohr | 107 | ²⁷⁰Bh | 61,0 s |
| Has | 108 | ²⁷⁰Hs | 40,0 s |
| Meitner | 109 | ²⁷⁸Mt | 8,0 s |
| Darmsztadt | 110 | ²⁸¹Ds | 11,0 s |
| Rentgen | 111 | ²⁸¹Rg | 26,0 s |
| Kopernik | 112 | ²⁸⁵Cn | 29,0 s |
| Nihon | 113 | ²⁸⁶Nh | 19,6 s |
| Flerow | 114 | ²⁸⁹Fl | 2,6 s |
| Moskow | 115 | ²⁸⁹Mc | 0,22 s |
| Liwermor | 116 | ²⁹³Lv | 0,061 s |
| Tenes | 117 | ²⁹⁴Ts | 0,078 s |
| Oganeson | 118 | ²⁹⁴Og | 0,0007 s |
Teoria atomowa przewiduje co prawda istnienie tzw. „wysp trwałości”, czyli szczególnie trwałych pierwiastków, które zawierałyby w jądrze określone liczby i proporcje protonów i neutronów. Trwałe miałyby być jądra „parzysto-parzyste” (czyli zawierające parzystą liczbę protonów i parzystą liczbę neutronów) i mające tzw. „magiczne liczby” tych cząstek. Zgodnie z tą hipotezą wyspa trwałości miała występować w okolicy pierwiastka 118 – tyle że to się za bardzo nie sprawdziło, bo akurat oganeson jest najmniej trwałym ze wszystkich znanych pierwiastków, a wyspa trwałości, i to zaledwie rzędu sekund, istnieje w okolicy rentgenu i koperniku. Tymczasem żeby można było pierwiastek znaleźć w przyrodzie, musi on mieć okres półtrwania rzędu setek tysięcy lat albo być nieustannie generowany przez jakiś ciągły proces. Problem w tym, że miejsca, w których takie procesy zachodzą, są wybitnie niezdrowe i na szczęście bardzo odległe od Układu Słonecznego. (Przy okazji uwaga językowa – nazwy pierwiastków traktujemy jako nieosobowe, stąd „u” w dopełniaczu. Dotyczy to także starszych pierwiastków: np. uranu i plutonu. Form „Urana” i „Plutona” używamy wtedy, gdy mowa o bogach lub planetach nazwanych ich imionami).
Zatem znalezienie pierwiastków cięższych od oganesonu jawi się jako wielce problematyczne, gdyż najprawdopodobniej będą one jeszcze mniej trwałe (i jeszcze trudniej będzie je wytworzyć w laboratorium). Załóżmy jednak, że dzięki procesom, których nauka jeszcze nie zna (co zawsze jest możliwe), powstają takie pierwiastki i są one na tyle trwałe, by dolecieć z miejsca, w którym powstały, na taką odległość od Ziemi, abyśmy mogli je wykryć. Czego należy szukać?
Dobrym i względnie łatwym do ustalenia parametrem jest gęstość, czyli zgodnie ze szkolną definicją, stosunek masy do objętości, a mówiąc bardziej praktycznie: masa jednostki objętości substancji. Układ metryczny jest tak sprytnie obmyślony, że gęstość wody wynosi 1 gram na centymetr sześcienny. Ilość energii potrzebna do ogrzania 1 grama wody o 1 stopień Celsjusza to 1 kaloria, zaś ilość energii, którą trzeba zabrać 1 gramowi wody, by ochłodzić go o 1 stopień Celsjusza to 1 frygoria (głównie w chłodnictwie).
Wróćmy jednak do tematu. Średnia gęstość Ziemi wynosi około 5,5 g/cm³ (inne planety skaliste Układu Słonecznego mają wartości zbliżone), średnia gęstość powietrza 0,0012 g/cm³. Dla porządku należałoby też dodać, w jakiej temperaturze, bo woda ma gęstość 1 g/cm³ tylko w temperaturze 4°C. W warunkach ziemskich gęstość podaje się zwykle dla temperatury pokojowej, za jaką uznawane jest 20°C. W kosmosie bywa zupełnie inaczej. Średnia gęstość Słońca to ok. 1,4 g/cm³ (co ciekawe, bardzo zbliżoną ma Jowisz), jednak im starsza jest gwiazda, tym większa jest jej gęstość. 1 cm³ białego karła (końcowego stadium życia małych i średnich gwiazd) waży ok. 100 ton, zaś 1 cm³ gwiazdy neutronowej (końcowego stadium życia masywnych gwiazd) – ok. 2 miliardów ton.
No dobrze, ale szukamy nowych pierwiastków, a nie egzotycznych rodzajów materii, z jakich składają się białe karły i gwiazdy neutronowe. Musimy więc patrzeć bliżej, bo białych karłów i gwiazd neutronowych nie mamy pod bokiem (na szczęście). W zasięgu dokładnej obserwacji pozostają w zasadzie ciała niebieskie wchodzące w skład Układu Słonecznego: planety, komety, asteroidy. Cała sprawa zaczęła się od artykułu B. Carry’ego z ESA, zatytułowanego „Density of Asteroids” i opublikowanego w czasopiśmie Planetary and Space Science (https://www.sciencedirect.com/journal/planetary-and-space-science). Co prawda miało to miejsce w 2012 roku, ale mainstreamowe media odkryły go dopiero niedawno, przynajmniej te polskie.
Zgodnie z tytułem artykuł dotyczy gęstości asteroid, małych ciał niebieskich, które w ogromnej acz nieokreślonej ilości pałętają się po całym Układzie Słonecznym, głównie w pasie między Marsem a Jowiszem. Wiele z nich zbliża się do Ziemi (jest to grupa zwana NEA, Near-Earth Asteroids) i może grozić kolizją – zdarzało się to w przeszłości wielokrotnie i miewało bardzo poważne konsekwencje. Dlatego tak ważny jest rozwój astronautyki, bo jeśli skupimy się wyłącznie na tym, co przynosi krótkoterminowy zysk elicie bogaczy, to możemy skończyć jak dinozaury.
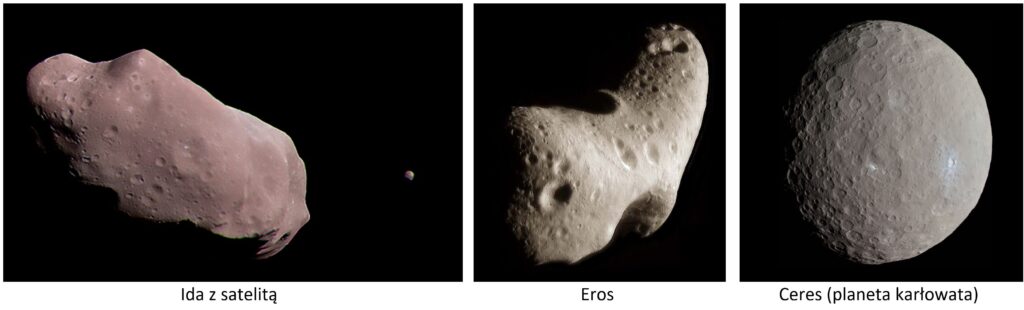
Asteroidy są uważane za pozostałości po planetezymalach, czyli ciałach niebieskich, z których w okresie przed 4,5 miliarda lat temu powstały planety. Mają najróżniejszy charakter – są wśród nich obiekty skaliste, lodowe, pyłowe, lodowo-pyłowe. Niektóre nie mają struktury zwartej, tylko porowatą albo stanowią wręcz stos niepołączonych ze sobą ściśle mniejszych i większych okruchów. Artykuł Carry’ego opisuje metody wyznaczania gęstości asteroid (co wymaga pomiaru ich objętości i oszacowania masy), ocenia ich wiarygodność i przedstawia duże zestawienie parametrów około 300 obiektów. Są to asteroidy pasa głównego (MBA od Main Belt Asteroid, czyli krążące po orbitach okołosłonecznych między Marsem a Jowiszem), bliskie Ziemi (NEA) oraz obiekty pozaneptunowe (TNO, Trans-Neptunian Object), czyli krążące dalej niż orbita Neptuna. Tabela zawiera też dane kilku komet, np. komety Halleya i Enckego.
Podane w artykule wartości gęstości mieszczą się w przedziale od 0,05 do 450,5 g/cm³. Dużo obiektów ma gęstość w okolicach 1 g/cm³, co oznacza najprawdopodobniej, że są zbudowane z lodu. Gęstość wyraźnie niższa od 1 wskazuje na porowatość, a wartości wyraźnie większe od 1 sugerują rosnącą zawartość metali. Bardzo rozpowszechnione w kosmosie żelazo ma gęstość ok. 7,9 g/cm³, lecz wiele asteroid ma większą, sięgającą 9, 10, a nawet kilkunastu gramów na centymetr sześcienny. Nas jednak szczególnie interesują te, których gęstość przekracza gęstość osmu, 22,6 g/cm³. Takich jest cztery, wszystkie MBA:
| Nazwa asteroidy | Średnica [km] | Gęstość [g/cm³] |
| Polihymnia | 54 | 75,28 |
| Atala | 60 | 47,92 |
| Ludmilla | 67,7 | 73,99 |
| De Sitter | 30,6 | 450,51 |
Być może należało dodać do tabeli jeszcze jedną kolumnę: niepewność oznaczenia. W przypadku Polihymni jest ona równa ok. 10 g/cm³ w każdą stronę, dla Ludmilli – 15, a dla De Sittera – 221! Czyli gęstość De Sittera może wynosić nawet ponad 670 g/cm³ – albo zaledwie 229. To i tak dużo, prawda? Tylko że tak wielka niepewność, sięgająca prawie 50%, powoduje, że otrzymany wynik jest bardzo mało wiarygodny. Autor artykułu sam przyznaje, że stosowane metody wyznaczania gęstości asteroid są niezbyt pewne, przede wszystkim ze względu na trudności w szacowaniu ich mas (wielkość daje się zmierzyć trochę lepiej). Także w przypadku mniejszych gęstości niepewność oznaczenia bywa duża, np. gęstość asteroidy o nazwie Prozerpina wynosi 1,98, a niepewność jej oszacowania 2,38.
Wartości podane w tabeli należą do grupy oznaczonej przez Carry’ego jako unrealistic. Dlaczego? Gęstość zależy od dwóch czynników: masy atomowej substancji oraz stopnia upakowania atomów w krysztale. Lecz jak już wiemy, im cięższy atom, tym mniej trwałe jego jądro. A w warunkach „normalnego” ciśnienia stopień upakowania nie może rosnąć w nieskończoność, z tych samych powodów, dla których bardzo ciężkie jądra atomowe są nietrwałe.
Kryształy metali (które stanowią większość pierwiastków) są zbudowane z jonów dodatnich, czyli atomów, od których odłączyła się przynajmniej część elektronów ostatniej powłoki (walencyjnych). Te jony dodatnie są spajane w całość przez opływającą je chmurę swobodnych elektronów o ładunku ujemnym (zwaną też czasem morzem elektronowym) – tych, które oderwały się od swoich atomów. Chmura elektronowa przyciąga dodatnie jądra do siebie, jednak (zgodnie z prawem Coulomba) im bliżej siebie się one znajdują, tym większa siła odpychania działa między nimi. W pewnym momencie ustala się równowaga między odpychaniem się jąder a ich przyciąganiem przez elektrony – i otrzymujemy trwały kryształ. Wniosek z tego, że istnieje ograniczenie, jeśli chodzi o stopień ścieśnienia jąder atomowych w krysztale (kto chce, może to spróbować obliczyć), czyli innymi słowy ograniczenie maksymalnej gęstości, jaką może spontanicznie uzyskać substancja w warunkach zbliżonych do normalnych. Weźmy też pod uwagę, że w kosmosie przeważa próżnia, a panujące w niej ciśnienie jest bliskie zeru.
Oczywiście przez zastosowanie większych ciśnień można pokonać ograniczenie upakowania. Tak właśnie powstaje wspomniana wyżej materia białych karłów i gwiazd neutronowych. Grawitacja ściska w nich materię do stanów ekstremalnych. W przypadku neutronium atomy „zapadają się w sobie” pod jej wpływem, elektrony łączą się z protonami i powstają neutrony. Zgodnie z nazwą, materia gwiazdy neutronowej składa się wyłącznie z neutronów – cząstek niemających ładunku elektrycznego. Takie cząstki można sprasować o wiele mocniej, gdyż brak rozpychających je sił elektrostatycznego odpychania (które działają między jądrami atomowymi mającymi ładunek dodatni). Nie należy jednak przesadzać z tą grawitacją, bo jak przesadzimy, to materia „zapadnie się” pod horyzont zdarzeń i dostaniemy czarną dziurę, a tego byśmy nie chcieli. Zatem istnieje w przyrodzie limit maksymalnej gęstości dla materii i jest nim właśnie gęstość neutronium.
Wracając do naszych asteroid – z uwagi na niewielkie masy tych obiektów panuje na nich mikroskopijne ciążenie i uzyskiwanie opisanych wyżej ekstremów jest niemożliwe. To dlatego fizycy uważają duże gęstości podane w ostatniej tabeli za nierealistyczne. Innymi słowy – prawie na pewno jest to błąd szacowania wynikający z niedoskonałości metody. Nie udało mi się znaleźć żadnego oszacowania, jaka byłaby maksymalna gęstość zwykłej materii w warunkach niezbyt wysokiego ciśnienia (powiedzmy w zakresie od próżni kosmicznej do 100 atmosfer; na powierzchni Wenus panuje ciśnienie ok. 91 atm). Jednak sądząc po tym, że mający największą gęstość osm nie jest najcięższym pierwiastkiem (więcej o tym na końcu), to nie przypuszczam, aby któryś z nieznanych pierwiastków miał gęstość mocno przekraczającą 25 g/cm³. Zakładając, że w ogóle da się je otrzymać w ilości umożliwiającej zmierzenie tego parametru.
Nie twierdzę oczywiście, że znalezienie w przyrodzie nieznanych jeszcze pierwiastków jest niemożliwe. Z tą niemożliwością w nauce trzeba uważać, a najlepiej w ogóle nie używać tego słowa. Koryfeusze nauki i filozofii nieraz się już w ten sposób zbłaźnili. W XVIII wieku członkowie Akademii Francuskiej, którym doniesiono o upadku meteorytu, stwierdzili, że kamienie nie mogą spadać z nieba, bo w niebie nie ma kamieni. W 1821 roku francuski pozytywista August Comte wątpił, czy człowiek będzie kiedyś w stanie poznać skład Słońca i gwiazd(sic), tymczasem już w 1825 roku stworzono podwaliny spektroskopii, metody pozwalającej wyznaczyć skład świecącego ciała przez badania emitowanego przez nie światła. Pod koniec XIX wieku niektórzy inżynierowie twierdzili, że nie da się zbudować maszyny latającej cięższej od powietrza, a niektórzy chemicy wątpili w istnienie jonów i prześladowali twórcę koncepcji dysocjacji jonowej, Arrheniusa.
Zatem tak, znalezienie w przestrzeni kosmicznej nieznanych pierwiastków jest możliwe, tyle że bardzo mało prawdopodobne. Nawet jeśli rzeczywiście one gdzieś we Wszechświecie powstają, to znikają w tempie ekspresowym, zaś ewentualne spektroskopowe sygnały ich istnienia mają zbyt niskie natężenie, byśmy mogli je wykryć. Już prawdopodobniejsze jest, że nowe pierwiastki otrzymamy w laboratoriach fizycznych na Ziemi. Niestety ich wytwarzanie będzie wymagało nowych, potężniejszych, a zatem większych i bardziej kosztownych akceleratorów. A kto by się tam przejmował finansowaniem drogich zabawek dla fizyków, skoro można maksymalizować zyski i akumulować kapitał…
Na koniec trzeba dodać, iż założenie, że nieznane pierwiastki muszą mieć gęstość większą od znanych, jest nieuzasadnione. Osm znajduje się w 6. okresie i ma liczbę atomową 76. Aż 37 następujących po nim pierwiastków o większej liczbie atomowej (w tym 16 występujących w przyrodzie) ma gęstość mniejszą! Wyjątek stanowi tylko pięć pierwiastków o liczbie atomowej 106–110, z tym że w ich przypadku są to jedynie szacunki, ponieważ nie otrzymano ich jeszcze w takiej ilości, by zbadać gęstość doświadczalnie.
Zatem tak, jeśli znajdziemy coś o gęstości większej od gęstości osmu, to może to wskazywać na obecność nieznanego pierwiastka – ale równie dobrze nowe pierwiastki mogą być ukryte w obiektach w ogóle niewyróżniających się gęstością. Zresztą zawartość nieznanych pierwiastków może być niewielka, a wtedy nawet jeśli będą miały dużą gęstość, to ich wpływ na średnią gęstość obiektu będzie znikomy. Innymi słowy – nic pewnego nie wiadomo, ale to przecież nie generuje kliknięć.
[źródła: B. Carry „Density of Asteroids”, Planetary and Space Science 73 (2012) 98–118; https://en.wikipedia.org/wiki/List_of_chemical_elements i hasła poświęcone poszczególnym pierwiastkom wymienionym w tekście; https://www.quora.com/Theoretically-what-is-the-maximum-density-possible-for-matter-in-context-of-a-black-hole; https://en.wikipedia.org/wiki/Maximum_density; https://pl.wikipedia.org/wiki/Auguste_Comte; https://en.wikipedia.org/wiki/Asteroid; https://www.esa.int/About_Us/ESAC; https://www.angstromsciences.com/density-elements-chart]
[źródła ilustracji: Periodictableru www.periodictable.ru – Own work, CC BY 3.0, https://commons.wikimedia.org/w/index.php?curid=9774411; Kevin Gill from Nashua, NH, United States – 243 Ida – August 1993, CC BY-SA 2.0, https://commons.wikimedia.org/w/index.php?curid=45862887; NASA/JPL/JHUAPL – http://photojournal.jpl.nasa.gov/catalog/PIA02923 (image link), Public Domain, https://commons.wikimedia.org/w/index.php?curid=45999926; By Justin Cowart – Ceres – RC3 – Haulani Crater, Public Domain, https://commons.wikimedia.org/w/index.php?curid=49700320; wiodąca: Photo 226410 © Dana Rothstein | Dreamstime.com]