
Aerożele są materiałami znanymi od około 100 lat, przynajmniej jeśli chodzi o odmiany otrzymane sztucznie. Od czasu do czasu jednak robi się wokół nich więcej medialnego szumu, co łatwo zrozumieć, bo ich właściwości bywają naprawdę nietypowe i potencjalnie użyteczne. Czasem jednak twórcy nagłówków przesadzają – tu zaliczyłbym np. artykuł opublikowany w sierpniu na stronie „Komputer Świat” pod sensacyjnym tytułem „Jest lżejszy od powietrza”.

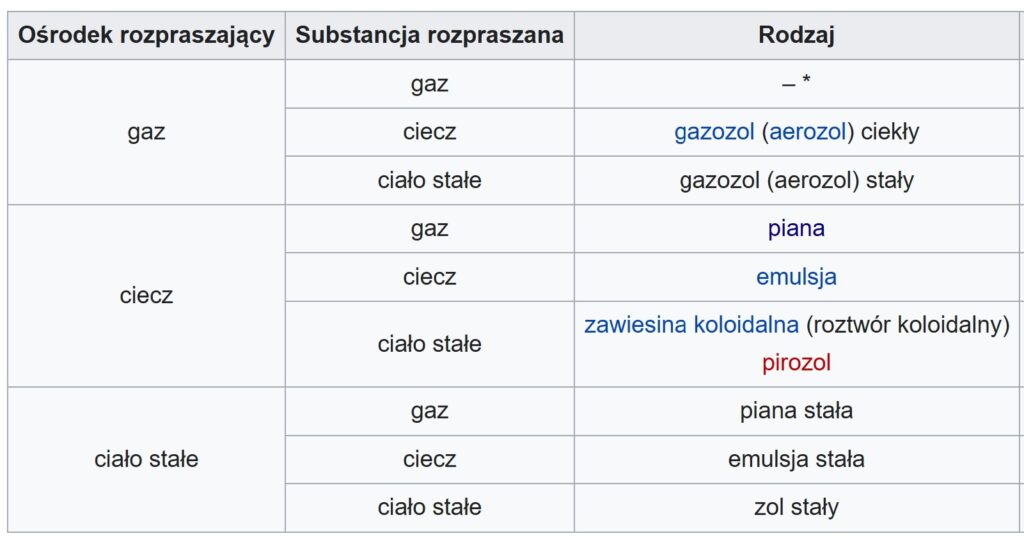
Zacznijmy od tego, czym jest właściwie aerożel. Jest to oczywiście jeden z rodzajów mieszanin. Mówiąc fachowo, aerożel jest układem dyspersyjnym, w którym fazą rozproszoną jest gaz, a fazą rozpraszającą – ciało stałe. Jeśli spojrzymy na klasyfikację układów koloidalnych (tabela), to znajdziemy taką kombinację pod nazwą „piana stała”. Różni się ona od częściej spotykanej przez nas zwykłej piany tym, że w tej ostatniej fazą rozpraszającą jest ciecz.
Pianę stałą znajdziemy w przyrodzie! Podanemu wyżej opisowi odpowiada np. pumeks, czyli skała wulkaniczna, która unosi się na wodzie. Pumeks powstaje przy szybkim ochłodzeniu nagazowanej lawy i składa się głównie z kwarcu i skaleni – oraz „pustych” pęcherzyków, zawierających przede wszystkim dwutlenek węgla i parę wodną. Te pęcherzyki zmniejszają jego gęstość i zapewniają mu pływalność, która wynika z tego, że pumeks jest „lżejszy” od wody. Gęstość pumeksu zależy od jego budowy, niektóre okazy mają np. gęstość 0,25 g/cm³. Innym przykładem piany stałej jest styropian, tworzywo sztuczne wyróżniające się niezwykle małą gęstością (0,11–0,32 g/cm³).


A co leży u podstaw potocznego określenia, że coś jest lżejsze/cięższe od wody lub powietrza? Odpowiedź jest prosta: porównanie gęstości. W przypadku gazów fizyk czy chemik dysponuje błyskawiczną metodą ustalenia, które są lżejsze, a które cięższe od powietrza. Wystarczy do tego pamiętać, że – z całkowicie wystarczającym przybliżeniem – wszystkie gazy mają jednakową objętość molową, czyli zamiast uczyć się na pamięć gęstości, wystarczy porównać masy molowe gazów, a do tego pamiętać, że średnia masa molowa suchego powietrza wynosi ok. 28,97 g/mol. A mas molowych nie trzeba zakuwać, bo można je obliczyć w prosty sposób na podstawie wzoru cząsteczkowego gazu i mas molowych pierwiastków, które można znaleźć np. w układzie okresowym. Widać stąd, że np. wodór (2 g/mol), hel (4 g/mol), metan CH₄ (16 g/mol) i amoniak NH₃ (17 g/mol) są lżejsze od powietrza, azot (28 g/mol) jest prawie tak samo ciężki jak powietrze (co nie dziwi, skoro to jego główny składnik), natomiast tlen (32 g/mol), siarkowodór H₂S (34 g/mol), dwutlenek węgla (44 g/mol) czy chlor (71 g/mol) są cięższe od powietrza. Balonik napełniony powietrzem wydychanym z płuc będzie opadać na ziemię, bo takie powietrze ma zwiększone stężenie CO₂.
W przypadku kwestii, czy dana ciecz lub ciało stałe jest lżejsze, czy cięższe od wody, mamy już trochę trudniej. Choć wszyscy chyba pamiętamy, że gęstość wody wynosi 1 g/cm³, gęstości cieczy i ciał stałych mają bardzo różne wartości i nie ma tam jednej „gęstości molowej”. Są i takie substancje ciekłe i stałe, których gęstość jest mniejsza od gęstości wody, i takie których gęstość jest większa.
Zatem jeśli mamy stwierdzić, czy dana ciecz lub ciało stałe jest lżejsze, czy cięższe od powietrza, musimy porównać gęstości. Gęstość powietrza (czyli atmosfery ziemskiej) zależy od wysokości, ciśnienia i temperatury. Pod ciśnieniem atmosferycznym, na poziomie morza i w temperaturze 20 °C średnia gęstość powietrza wynosi ok. 1,2 kg/m³, co odpowiada 1,2 g/dm³ albo 1,2 mg/cm³. Czyli jest bardzo niska i – być może ku naszemu rozczarowaniu – prawie wszystkie substancje stałe i ciekłe mają większą gęstość, a zatem nie mogą „unosić się w powietrzu”.
Aerożele są jednak materiałami niezwykle lekkimi. Tak się przynajmniej o nich pisze w mediach. Ale co to właściwie oznacza? Aerożel składa się ze stałego szkieletu („ścianek” piany) i gazu znajdującego się w jego lukach pęcherzyków. Jeśli będzie to powietrze, logika sugeruje, że gęstość aerożelu, aczkolwiek mała, będzie jednak większa od gęstości powietrza, nawet gdy wskaźnik porowatości aerożelu (czyli stosunek zawartości gazu do całości materiału) jest wysoki. Aerożele zwykle mają porowatość od 50 do 99,8%, jednak nawet te o największej wartości tego wskaźnika mają gęstości rzędu kilku gramów na decymetr sześcienny, a rekordzista ma gęstość 1,9 g/dm³. Czyli są jednak cięższe od powietrza.


Rozwiązanie podpowiada nam historia baloniarstwa. Kiedy bracia Montgolfier przeprowadzili pierwsze próby z balonem na ogrzane powietrze i przesłali ich opis do Akademii Francuskiej, do Paryża, uczony Jacques Charles, któremu Akademicy zlecili zbadanie sprawy, wykazał się tak zwanym twórczym lenistwem. Nie miał specjalnej ochoty podróżować na daleką francuską prowincję, a będąc specjalistą od właściwości gazów, wydedukował, że bracia musieli napełnić swój balon gazem lżejszym od powietrza. Taki gaz był wtedy już znany: wodór.
Zatem mamy dwa sposoby, aby aerożel stał się rzeczywiście „lżejszy od powietrza”: można rozrzedzić zawarte w nim powietrze, ogrzewając go, albo zastąpić je inną substancją, o odpowiednio małej gęstości. Skrajnym przypadkiem będzie tu całkowite opróżnienie porów w aerożelu, by zapanowała w nim próżnia. Rozwiązanie to nie jest praktyczne w przypadku balonów: balon „na próżnię” miałby rzeczywiście korzystną aerostatykę, w dodatku próżnia, w odróżnieniu od wodoru, jest niepalna – jednak jego ścianki musiałyby być bardzo grube, by oprzeć się ciśnieniu atmosferycznemu, a to zbyt mocno zwiększyłoby jego ciężar.
W przypadku aerożelu ścianki pęcherzyków są sztywne i bez problemu wytrzymują napór ciśnienia atmosferycznego – w końcu aerożel jest klasyfikowany jako „piana stała”. I rzeczywiście udało się otrzymać „próżniowy” aerożel o gęstości ok. 1,0 g/dm³, a zatem mniejszej od gęstości powietrza. Podobny efekt można też osiągnąć, ogrzewając materiał. Zatem tak, w pewnych warunkach aerożel może być lżejszy od powietrza!
Sztuczne aerożele otrzymuje się ze specjalnie przygotowanych układów ciekłych, z których odpowiednią metodą usuwa się ciecz (np. przez wymrażanie). Fazą stałą aerożelu mogą być np. krzemionka, tlenki metali (m.in. glinu, tytanu, żelaza, wanadu, samaru), węgiel albo niektóre polimery. Pierwszy sztuczny aerożel został otrzymany przez amerykańskiego chemika Samuela Stephensa Kistlera pod koniec lat 20. XX wieku. Podobno Kistler zajął się tym zagadnieniem w wyniku zakładu: jeden z jego kolegów zażądał zastąpienia fazy ciekłej gazową bez zniszczenia struktury fazy stałej (legenda głosi, że problem dotyczył nieokreślonej bliżej „galaretki” albo żelków, ang. jellies).

Musiało minąć kilkadziesiąt lat, nim udało się opracować bardziej praktyczne metody otrzymywania aerożeli. Szybko się wtedy okazało, że mają one – prócz niewielkiej gęstości – także wiele innych korzystnych właściwości. Znakomicie sprawdzają się jako izolacja cieplna (publikowano np. zdjęcia nietopniejącej kostki lodu znajdującej się na aerożelu, który był z kolei umieszczony nad płomieniem palnika), są silnie higroskopijne i mają bardzo dużą wytrzymałość mechaniczną jak na swoją masę. Ich zastosowania wiążą się głównie z tymi właściwościami, choć używano aerożeli także do bardziej nietypowych celów. Wykorzystywano je na przykład do transportu leków w organizmie albo jako pochłaniacze pyłu kosmicznego w sondach kosmicznych. Astronautyka zresztą będzie jeszcze sięgać po aerożele wielokrotnie.


Tekst opublikowany pierwotnie na facebookowej grupie wydawnictwa Nowa Era „Chemia dla nauczycieli”.
[źródła: https://en.wikipedia.org/wiki/Aerogel; https://en.wikipedia.org/wiki/Colloid; https://en.wikipedia.org/wiki/Pumice; https://en.wikipedia.org/wiki/Atmosphere_of_Earth; B. Orłowski „Przygody latającej bani”, seria „Niezwykłe sprawy zwykłego świata”, Krajowa Agencja Wydawnicza, Warszawa 1967; https://www.komputerswiat.pl/artykuly/redakcyjne/czy-istnieje-cos-lzejszego-od-powietrza-okazuje-sie-ze-tak/hhpbzfp]
[źródła ilustracji: Aerogelflower.jpg: No information.derivative work: JovanCormac – Aerogelflower.jpg, Public Domain, https://commons.wikimedia.org/w/index.php?curid=7424463; NASA/JPL-CalTech; https://makezine.com/article/digital-fabrication/3d-printing-workshop/how-to-build-a-supercritical-dryer-and-make-your-own-aerogel/; NASA/JPL-Caltech – NASA Stardust Website, Public Domain, https://commons.wikimedia.org/w/index.php?curid=35154; NASA/JPL-Caltech – NASA Stardust Website, Public Domain, https://commons.wikimedia.org/w/index.php?curid=85519; kanał Nintendo Kid https://www.youtube.com/watch?v=L9zwCm7QHRc&ab_channel=NintendoKid]